روز جهانی تالاسمی

اپیدمیولوژی تالاسمی
بیماری تالاسمی، شایع ترین شکل کم خونی ارثی است که به دلیل اختلال در سنتز یکی از دو زنجیره گلوبین در هموگلوبین ایجاد می شود. مشخص شده است که این اختلال در مناطق گرمسیری و نیمه گرمسیری جهان (به عنوان مثال، جنوب شرقی آسیا، منطقه مدیترانه، شبه قاره هند و آفریقا) بسیار شایع است.
در سال های اخیر به دلیل افزایش جمعیت مهاجر، تعداد بیماران تالاسمی در سایر مناطق جهان از جمله در آمریکای شمالی، شمال اروپا و شمال شرقی آسیا در حال افزایش بوده است

انواع تالاسمی
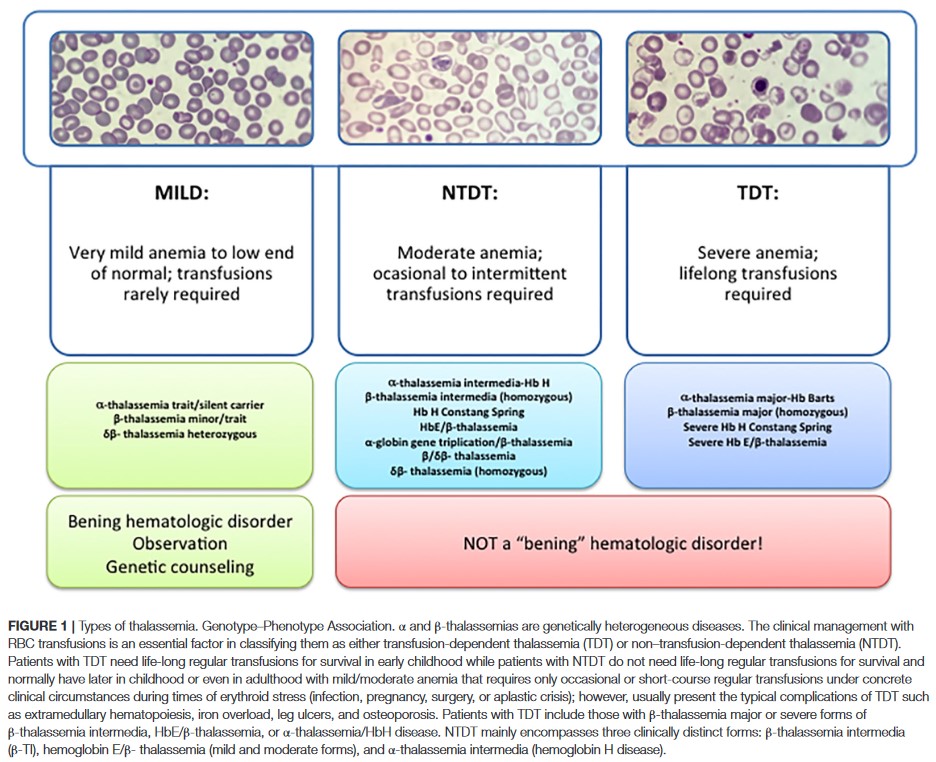
در سال 2012، فدراسیون بین المللی تالاسمی اصطلاحات جدیدی را برای طبقه بندی بالینی تالاسمی اتخاذ کرد: ransfusion-dependent thalassemia (TDT) و non–transfusion-dependent thalassemia (NTDT) که در سه نوع مختلف گروه بندی می شود:
- α-thalassemia intermedia (hemoglobin H disease)
- β-thalassemia intermedia (β-TI)
- hemoglobin E/β- thalassemia (mild and moderate forms)
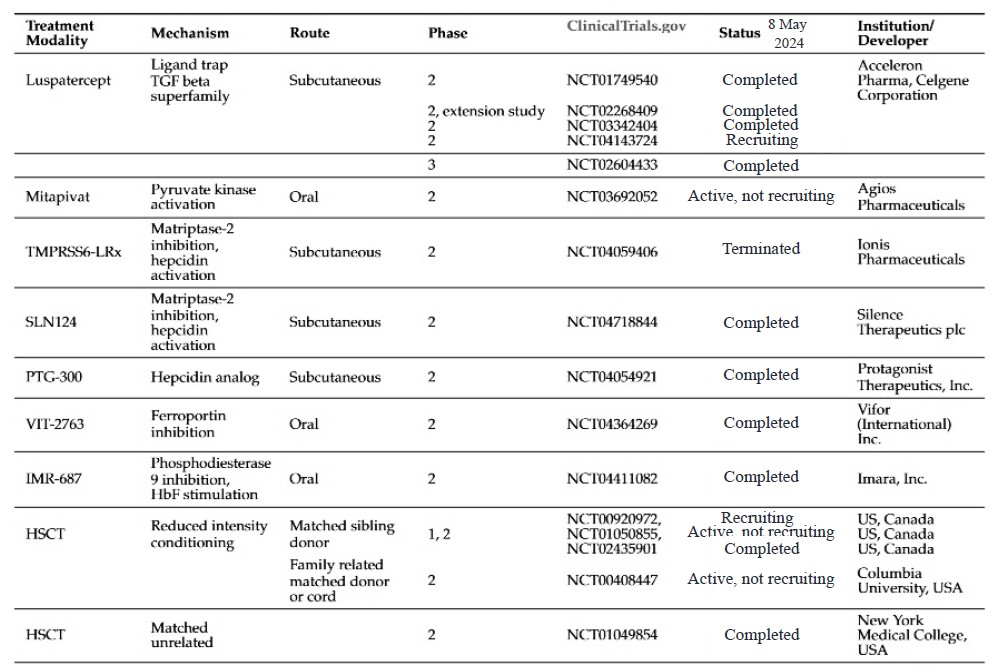
جدیدترین رویکردهای درمانی تالاسمی
- Allogeneic Hematopoietic Stem Cell Transplantatio
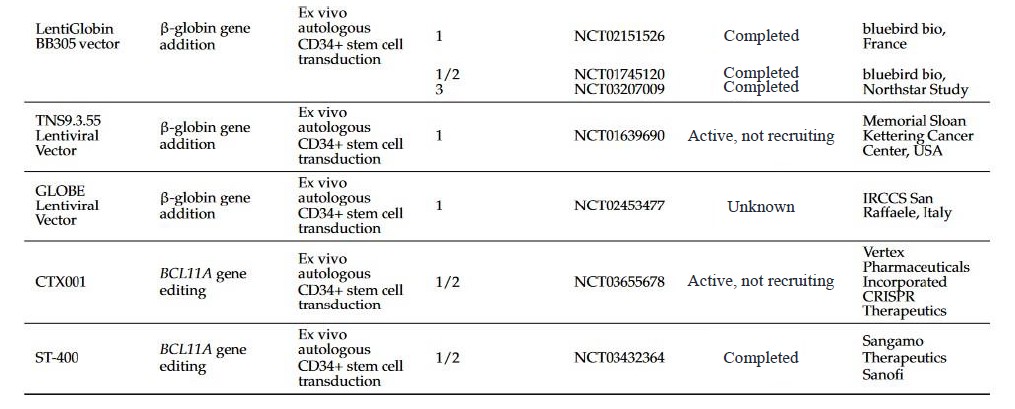
- Gene Therapy
- Gene Addition
- Gene Editing
جدیدترین رویکردهای غیردرمانی تالاسمی (Disease-Modifying)
- The TGF-β (Transforming Growth Factor-β) Superfamily Ligand Traps
- Pyruvate Kinase Activation
- Phosphodiesterase 9 Inhibition
- Iron Metabolism Manipulation

جدیدترین درمان های تایید شده برای بیماران تالاسمی
2019: سازمان غذا و داروی ایالات متحده Reblozyl (luspatercept-aamt) را برای درمان کم خونی بزرگسالان مبتلا به بتا تالاسمی که نیاز به تزریق مکرر گلبول قرمز دارند، تأیید کرد.
2019: Sotatercept™ توسط سازمان غذا و داروی ایالات متحده برای درمان کم خونی در بیماران وابسته به انتقال خون مبتلا به بتا تالاسمی تایید شد.
2021: Chiesi Global Rare Diseases دریافت تاییدیه FERRIPROX™ را برای بیماران Transfusional Iron Overload به دلیل بیماری آنمی داسی شکل اعلام کرد.
2022: شرکت Bluebird bio اعلام کرد که ZYNTEGLO™ توسط سازمان غذا و داروی ایالات متحده تایید شده است. ZYNTEGLO™ که به نام beti-cel نیز شناخته می شود، یک one-time gene therapy است که به طور سفارشی برای درمان علت زمینه ای ژنتیکی بتا تالاسمی در بیماران بزرگسال و کودکانی که نیاز دارند، طراحی می شود.
2024: سازمان غذا و داروی ایالات متحده exagamglogene autotemcel (exa-cell، با نام تجاری Casgevy™) را برای درمان تالاسمی بتا وابسته به انتقال خون در بیماران 12 سال و بالاتر تایید کرد.
References